A manchete que assusta
"Canetas emagrecedoras destroem a massa muscular." Você provavelmente já viu alguma variação dessa frase em redes sociais, portais de saúde ou até em conversas entre colegas. A narrativa se espalhou rápido e com força, alimentada por dados reais dos grandes ensaios clínicos. Dependendo do estudo e da forma de análise, a proporção de massa magra perdida em relação ao peso total varia entre 25% e 40%. No SURMOUNT-1 com tirzepatida, a análise por DXA mostrou cerca de 26% de FFM. No substudo do STEP-1 com semaglutida, chegou a 40%. Números assim assustam — e deveriam mesmo chamar atenção.
Mas essa variação já revela um primeiro problema: a forma como os dados são apresentados muda drasticamente a percepção do risco. E há um problema ainda mais fundamental na interpretação. Ela confunde dois conceitos que parecem iguais mas não são: massa livre de gordura e músculo esquelético. Essa confusão não é exclusividade de leigos — ela aparece em matérias de jornais, em postagens de profissionais da saúde e até em discussões entre pesquisadores. E quando você entende a diferença, toda a narrativa muda.
Em setembro de 2024, Tinsley e Heymsfield publicaram um artigo no Journal of the Endocrine Society que aborda exatamente esse ponto. É um daqueles textos que não traz dados novos de um experimento, mas reorganiza o que já sabemos de forma que tudo passa a fazer mais sentido. O argumento central: estamos interpretando mal os dados de composição corporal — e isso está distorcendo a conversa sobre os GLP-1.
Massa magra não é músculo: o erro que distorce tudo
Para entender o que Tinsley e Heymsfield estão dizendo, precisamos dar um passo atrás e falar sobre como o corpo humano é analisado.
Na ciência da composição corporal, existe um modelo clássico chamado "modelo de 5 níveis", proposto por Wang et al. (1992). Esse modelo organiza o corpo em diferentes camadas de análise: atômico (elementos químicos), molecular (gordura, água, proteína, minerais), celular, tecido/órgão (músculo, osso, tecido adiposo), e corpo inteiro. Cada nível tem suas métricas e seus métodos de medição.
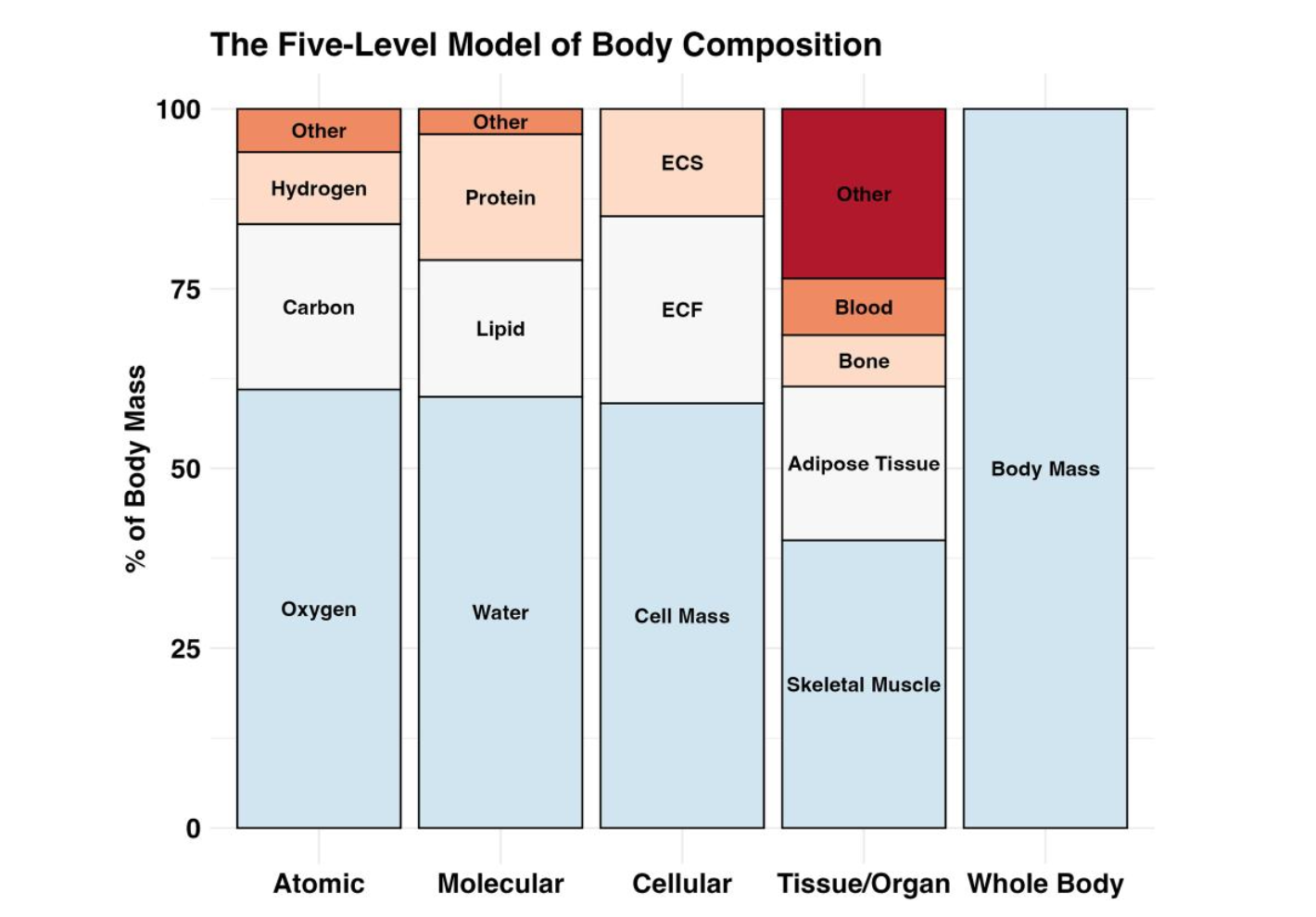
Quando fazemos um exame de DXA — o método mais comum nos estudos clínicos — estamos trabalhando no nível molecular. O DXA divide o corpo em massa gorda e massa livre de gordura (fat-free mass, ou FFM). E aqui está o ponto crucial: a FFM é simplesmente "tudo que não é gordura". Isso inclui água, proteína, minerais — onde quer que estejam no corpo. Não é um tecido específico. É uma categoria contábil.
Já o músculo esquelético é um tecido anatômico real, que pertence ao nível de tecido/órgão. É composto por cerca de 73% de água, 22% de proteína, além de minerais, gordura intramuscular e outros componentes. E aqui está o dado que muda a perspectiva: num homem de referência, a FFM pesa cerca de 56,5 kg, enquanto a massa muscular esquelética pesa cerca de 28 kg. Numa mulher de referência, são 42 kg de FFM contra 17 kg de músculo. Ou seja, a massa muscular corresponde a menos da metade da FFM total.
Quando um estudo reporta perda de 5 kg de FFM, portanto, não significa que foram 5 kg de músculo. A FFM inclui componentes de todos os tecidos do corpo — e para entender o que realmente acontece, precisamos abrir esse número.
A perda "obrigatória" que ninguém conta
Há um segundo conceito no artigo de Tinsley que é igualmente importante e raramente discutido: a perda obrigatória de FFM quando se perde tecido adiposo.
O tecido adiposo não é 100% gordura pura. Ele contém aproximadamente 80-85% de triglicerídeos, 15% de água e 5% de proteína. Há vasos sanguíneos, tecido conjuntivo, células imunes — todo um ecossistema que sustenta e irriga as células de gordura. E toda essa infraestrutura, do ponto de vista molecular, conta como massa livre de gordura.
O que isso significa na prática? Quando você perde 10 kg de tecido adiposo, automaticamente perde 1,5 a 2 kg de FFM que estavam dentro desse tecido. Não é músculo. É a "estrutura de suporte" da gordura que foi embora junto com ela. É inevitável — e é biologicamente esperado.
A analogia aqui é simples: imagine que você está demolindo parte de um prédio. Não tem como tirar só os tijolos e deixar a fiação elétrica, o encanamento e o reboco flutuando no ar. Quando a estrutura vai embora, a infraestrutura vai junto. Com o tecido adiposo é a mesma coisa.
Tinsley e Heymsfield demonstram isso matematicamente aplicando a correção aos dados dos principais trials de GLP-1. Quando você subtrai a FFM obrigatória perdida do tecido adiposo, o número de FFM "real" perdida de outros tecidos cai significativamente — e em alguns estudos, como o de Heise et al. (2023) com tirzepatida e o de Kadouh et al. (2020) com liraglutida, a FFM ajustada fica próxima de zero ou até levemente positiva.
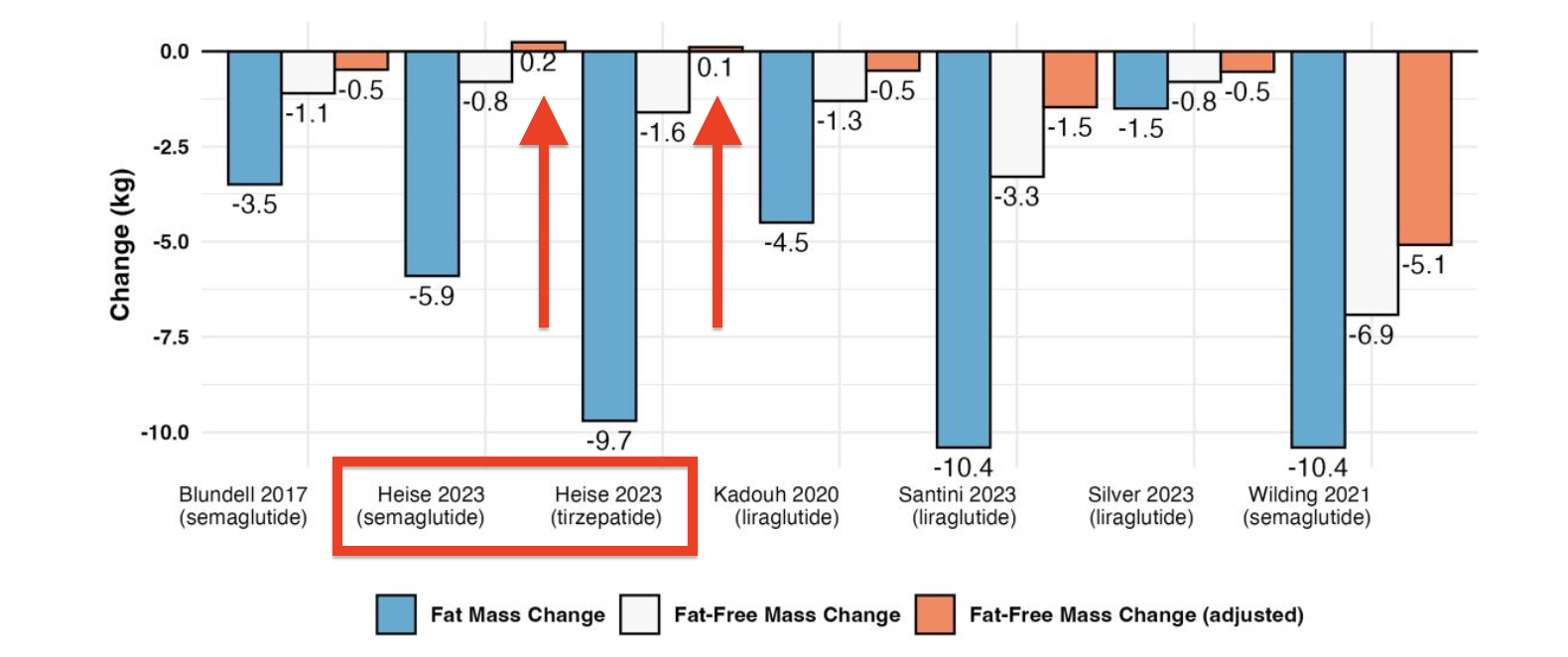
Quando o treino de resistência entra na equação, o efeito é ainda mais expressivo. Abe et al. (2019) mostraram que, ao aplicar essa mesma correção em intervenções de perda de peso com exercício resistido, a aparente perda de massa magra desaparecia por completo — e em alguns casos, se convertia em ganho.
De onde realmente vem a massa magra perdida
Mas mesmo depois dessa correção, ainda resta FFM perdida de tecidos não-adiposos. E aqui entra um estudo elegante que Tinsley cita: o trabalho de Bosy-Westphal et al., que usou ressonância magnética para identificar de onde vem a FFM perdida durante o emagrecimento.
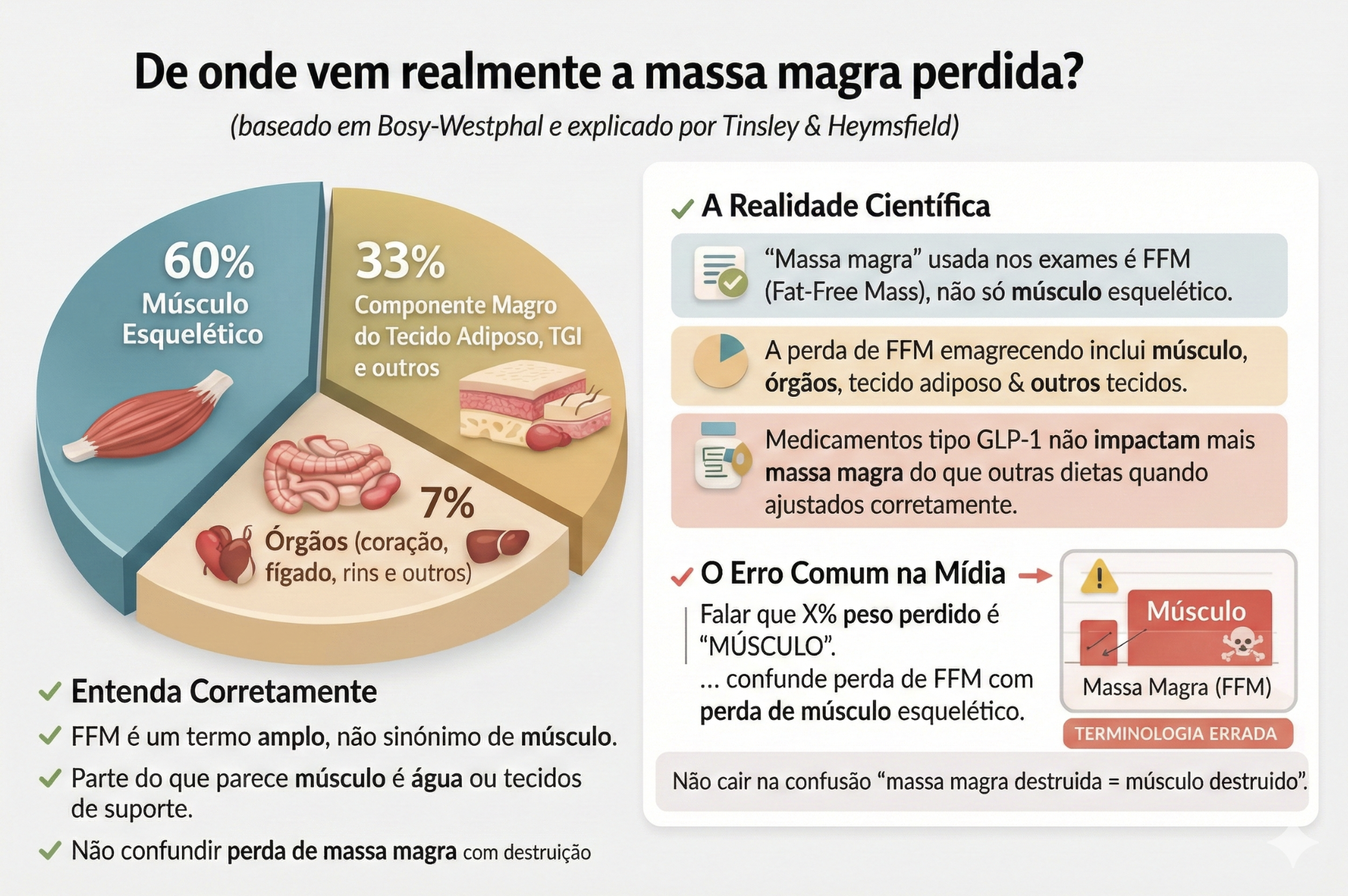
Em mulheres com sobrepeso e obesidade que perderam 9,5 kg, a perda de FFM foi de 1,5 kg. Quando os pesquisadores rastrearam a origem dessa perda, descobriram que 60% veio do músculo esquelético, 33% veio do componente magro do tecido adiposo, do trato gastrointestinal, da pele e de outros tecidos não mensurados, e 7% veio de órgãos como rim, coração e fígado.
E mesmo os 60% que vieram do músculo não são todos "músculo de verdade" no sentido que imaginamos. Quando Bosy-Westphal decompôs essa perda muscular, encontrou que 46% da FFM total perdida era água do músculo, e apenas 10% era proteína muscular propriamente dita.
Vamos traduzir isso para os números dos estudos com GLP-1. Se alguém perde 20 kg com tirzepatida e os dados reportam 5 kg de "perda de massa magra", a realidade é mais ou menos esta: parte dessa perda é obrigatória e veio do próprio tecido adiposo que foi embora, outra parte veio de órgãos e outros tecidos, boa parte do que veio do músculo era água, e a perda real de proteína muscular é uma fração do que os 5 kg sugerem.
Isso não significa que a perda muscular não existe ou não importa. Significa que os números estão sendo mal interpretados — e que a proporção de perda com GLP-1 parece seguir o mesmo padrão de qualquer outro método de emagrecimento, não sendo algo específico ou pior dessas medicações.
A proporção é a mesma — com ou sem medicamento
Esse é talvez o ponto mais importante para o profissional de Educação Física: a chamada "regra do quarto de FFM" (quarter FFM rule). Historicamente, a ciência observa que aproximadamente 25% do peso perdido tende a ser massa livre de gordura, independentemente do método utilizado.
Tinsley cita a revisão sistemática de Chaston et al., que comparou diferentes intervenções antes da era dos GLP-1: dietas de baixa caloria resultaram em 14% do peso perdido como FFM, dietas de muito baixa caloria em 23%, e intervenções cirúrgicas entre 18% e 31%. A mediana geral gira em torno dos 25%.
No SURMOUNT-1 com tirzepatida, a análise por DXA mostrou uma proporção de aproximadamente 74% de massa gorda e 26% de massa magra — praticamente idêntica ao grupo placebo, que perdeu muito menos peso total mas na mesma proporção. No STEP-1, o substudo de DXA com amostra menor reportou uma proporção maior de FFM (cerca de 40%), mas essa diferença pode refletir variações no tamanho da amostra e no método de análise, não necessariamente um efeito biológico diferente.
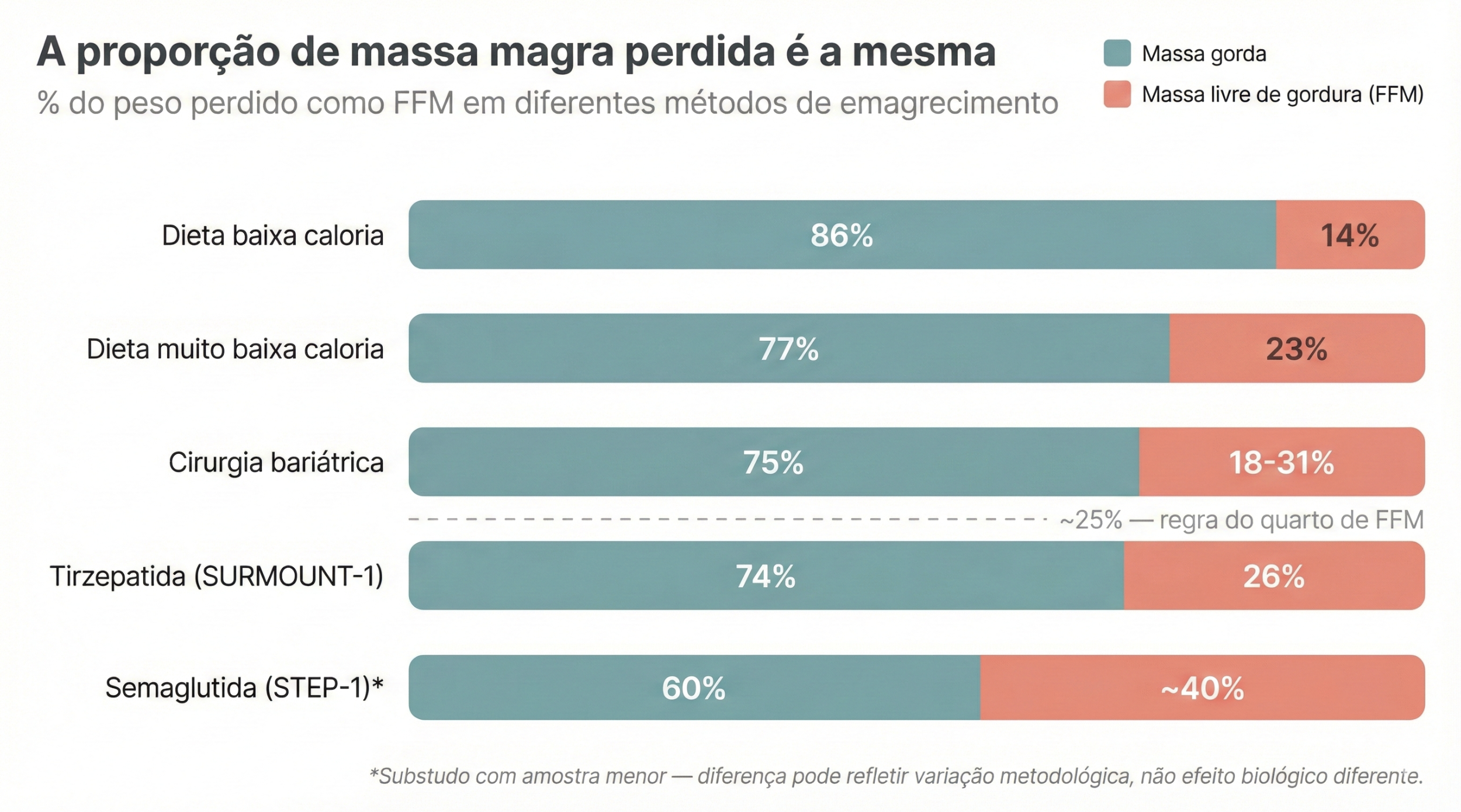
O que isso nos diz é claro: os GLP-1 não são especialmente "destruidores de músculo". Eles produzem perdas de peso maiores, e portanto perdas absolutas de FFM maiores, mas a proporção relativa é consistente com o que se observa em qualquer outro déficit calórico. A biologia do emagrecimento funciona da mesma forma independentemente de como o déficit é criado. Como Tinsley e Heymsfield colocam explicitamente: comparações diretas dentro de ensaios contemporâneos ainda são necessárias para confirmar essa similaridade, mas o padrão geral é consistente com o que se observa em outros métodos.
Mas a preocupação não é infundada
Dizer que os números estão sendo mal interpretados não é o mesmo que dizer que não há motivo para preocupação. Há — e motivo sério.
Uma revisão publicada na Obesity Reviews por Mechanick et al. (2024), com o próprio Heymsfield como coautor, estima que os participantes do STEP-1 e do SURMOUNT-1 perderam pelo menos 10% da massa muscular total em 68 a 72 semanas de tratamento. Para colocar em perspectiva, isso equivale a aproximadamente 20 anos de perda muscular associada ao envelhecimento normal em adultos após os 30 anos, que é estimada em 3-5% por década.
Esse dado é importante porque contextualiza a magnitude do problema. A perda pode seguir a mesma proporção de qualquer emagrecimento, mas quando a perda total de peso é de 15-20%, o valor absoluto de músculo perdido não é trivial. E para certas populações — idosos, pessoas com baixa massa muscular prévia, mulheres na menopausa — isso pode ter impacto funcional real.
Mechanick e colegas fazem ainda outro alerta relevante: muitas pessoas com obesidade já partem de uma ingestão proteica inadequada. Quando o GLP-1 reduz drasticamente o apetite, a tendência é que essa ingestão caia ainda mais. Se o paciente não está comendo proteína suficiente e não está treinando força, a perda muscular pode ser significativamente pior do que a média dos estudos.
A preocupação é tão séria que a própria comunidade científica já discute a necessidade de terapias farmacológicas complementares para proteger o músculo durante o uso de GLP-1. Uma revisão recente de Hierholzer et al. (2026) mapeou o pipeline de candidatos — de moduladores seletivos de receptores androgênicos a inibidores de miostatina e terapias de silenciamento gênico — reconhecendo que, apesar de dados pré-clínicos promissores, as limitações ainda são grandes: trials curtos, poucos dados funcionais e dependência de biológicos injetáveis. E um workshop recente da Society on Cachexia and Wasting Disorders (SCWD) com a FDA (von Haehling et al., 2025) discutiu os desafios regulatórios e clínicos para definir endpoints adequados para medir preservação muscular durante terapias de perda de peso — um sinal de que o problema está sendo levado a sério nas mais altas esferas.
O músculo que fica pode ser um músculo melhor
Se a narrativa até aqui foi sobre redimensionar a preocupação, agora vem um ângulo que praticamente ninguém está discutindo: os GLP-1 podem estar melhorando a qualidade do músculo que permanece.
Uma revisão recente publicada no European Journal of Clinical Investigation por De Girolamo et al. (2025) compilou evidências pré-clínicas e clínicas iniciais mostrando que os agonistas de GLP-1 promovem melhora no recrutamento microvascular do músculo (mais sangue chegando nas fibras), aumento da eficiência mitocondrial (o músculo gera energia de forma mais eficiente), e redução da gordura intramuscular — a chamada mioesteatose. Os autores concluem que o efeito dos GLP-1 no músculo parece ser mais de melhora de qualidade do que de hipertrofia, o que é uma distinção importantíssima.
O estudo SEMALEAN, publicado no Diabetes, Obesity & Metabolism em 2025 (Alissou et al., 2025), trouxe dados clínicos que corroboram essa ideia. Neste estudo prospectivo com 106 pacientes usando semaglutida 2,4 mg por 12 meses, os resultados mostraram que a massa magra caiu inicialmente (cerca de 3 kg nos primeiros 7 meses), mas estabilizou depois. Enquanto isso, a força de preensão manual aumentou 4,5 kg aos 12 meses, a prevalência de obesidade sarcopênica caiu de 49% para 33%, e o gasto energético de repouso normalizado pela massa magra aumentou entre o 7º e o 12º mês.
Pense nisso: mesmo com menos massa magra no total, os pacientes ficaram mais fortes. É como se o corpo estivesse fazendo uma "reforma interna" — tirando o que não serve (gordura infiltrada no músculo, tecido de baixa qualidade) e melhorando o que fica. Essa é uma mensagem que muda completamente o tom da conversa com o seu aluno.
Uma revisão publicada na Current Opinion in Endocrinology, Diabetes and Obesity (Bhandarkar et al., 2025) complementa essa perspectiva: os GLP-1RAs produzem redução preferencial de gordura visceral, os declínios na massa magra são modestos e proporcionais, o gasto energético de repouso é mantido — com relatos de aumento durante terapia prolongada — e dados em roedores mostram efeitos protetores no músculo via mecanismos anti-inflamatórios e miogênicos.
E há um dado adicional que merece destaque: quando o medicamento é interrompido e o reganho de peso acontece, a recomposição tende a ser primariamente de gordura — o que reforça brutalmente a importância de ter preservado o máximo de músculo possível durante o tratamento.
O elefante na sala: você provavelmente não é o público dos estudos
Tudo o que discutimos até agora se baseia em estudos com populações específicas. E aqui está um ponto que quase ninguém está levantando, mas que é fundamental para quem atende mulheres no consultório ou no estúdio.
Os critérios de inclusão dos grandes ensaios são claros: SURMOUNT-1 incluiu pessoas com IMC ≥30, ou ≥27 com pelo menos uma comorbidade. Os estudos STEP seguiram a mesma lógica. O estudo SEMALEAN tinha um IMC médio de 46,3 kg/m² — obesidade grave. Todos esses estudos foram desenhados para tratar obesidade como doença, em populações que têm muito tecido adiposo para perder.
Mas o uso real está acontecendo em populações completamente diferentes.
Quando busquei na literatura estudos com mulheres com peso normal ou leve sobrepeso usando GLP-1, não encontrei nenhum ensaio clínico controlado. O que encontrei foi um relato de caso — publicado no Endocrinology, Diabetes & Metabolism Case Reports — de uma mulher de 37 anos com IMC normal que usou semaglutida por motivos cosméticos, sem supervisão médica, e desenvolveu obstrução intestinal. Um caso isolado, mas revelador da realidade de uso.
Quando busquei estudos específicos em mulheres na pré, peri ou pós-menopausa, o cenário foi igualmente vazio. Encontrei uma revisão mecanística sobre o papel dos GLP-1 na osteosarcopenia (Tufail et al., 2025) que menciona mulheres pós-menopausa, mas é teórica — não um ensaio clínico. E há um protocolo de estudo em andamento (Cortes et al., 2024) avaliando semaglutida em adultos ≥65 anos com IMC entre 27 e 40, mas os resultados ainda não foram publicados.
A conclusão é inescapável: a ciência tem uma lacuna enorme para as populações que mais estão usando esses medicamentos fora das indicações originais.
Por que isso é especialmente preocupante para mulheres 40+
Uma mulher de 45-55 anos que não é clinicamente obesa mas usa GLP-1 para perder "aqueles 5-8 kg" está numa situação biologicamente muito diferente de uma pessoa com IMC 45. E essa diferença importa.
Primeiro, ela já está perdendo músculo naturalmente. A queda de estrogênio que acompanha a perimenopausa e a menopausa está associada a declínio progressivo de massa muscular e força. É um processo fisiológico que acontece independentemente de qualquer medicamento.
Segundo, ela tem menos "reserva" de massa magra para perder. Uma pessoa com obesidade grave pode perder uma quantidade significativa de FFM e ainda ter massa muscular funcional adequada. Uma mulher com IMC 26 que já não treina força pode não ter essa margem.
Terceiro, a proporção de perda pode ser diferente. Nos estudos com obesos, grande parte da FFM perdida vem do componente magro do tecido adiposo — porque há muito tecido adiposo para perder. Numa mulher com pouca gordura visceral, essa "proteção" proporcional não existe da mesma forma. A fração de perda que vem efetivamente do músculo pode ser proporcionalmente maior.
Quarto, o impacto funcional é amplificado. Perder 2 kg de massa muscular quando você tem 30 kg de músculo total é diferente de perder 2 kg quando você tem 15 kg. A reserva funcional menor significa que cada quilograma perdido pesa mais — literalmente e figurativamente.
E há um quinto ponto que raramente entra na discussão: não sabemos como os GLP-1 interagem com as alterações hormonais da menopausa no que diz respeito ao metabolismo muscular. Os efeitos protetores documentados nos estudos com obesos podem ser diferentes numa mulher com perfil hormonal diferente. Simplesmente não temos dados.
A mensagem honesta que quase ninguém está dando é esta: se você não é clinicamente obeso, se o seu IMC está entre 24 e 28, se você está na perimenopausa ou menopausa — você não é o público dos estudos. Não sabemos o que acontece com a sua composição corporal. Extrapolar os dados de populações com obesidade grave para essa realidade é especulação, e pode ser uma especulação perigosa.
O papel do treino de força: a variável que você controla
Se há uma mensagem que une todos os estudos — dos que analisam mecanismos moleculares aos que avaliam desfechos clínicos — é esta: treino de resistência e ingestão adequada de proteína são as duas contramedidas mais eficazes para preservar massa muscular durante qualquer processo de emagrecimento, com ou sem medicamento.
Tinsley e Heymsfield dedicam a seção final do artigo a esse ponto. Eles citam dados mostrando que 81% das intervenções de restrição calórica sem exercício resultaram em mais de 15% do peso perdido como FFM, contra apenas 39% quando o exercício foi incluído. E quando o exercício era treino de resistência, os resultados de preservação muscular foram consistentemente superiores.
No contexto específico dos GLP-1, o estudo de Lundgren et al. (2021) é particularmente relevante. Participantes que combinaram liraglutida com exercício tiveram redução de gordura corporal de 3,9 pontos percentuais — aproximadamente o dobro dos grupos que usaram exercício ou liraglutida isoladamente. E no follow-up após parar os tratamentos, os grupos que haviam feito exercício tiveram manutenção superior do peso e da composição corporal — o exercício protegeu mesmo depois que tudo parou.
Mechanick et al. reforçam que a proteína deve estar entre 1,2 e 1,6 g/kg de peso corporal por dia, distribuída em múltiplas refeições, com foco em fontes de alta qualidade. Isso é especialmente importante com GLP-1 porque a redução de apetite pode levar a ingestão proteica insuficiente se não houver planejamento deliberado. Um ponto prático: oriente seu aluno a planejar a proteína primeiro e construir o restante da refeição em torno dela. Quando o apetite está reduzido, cada garfada conta.
Para o personal trainer, isso se traduz em um mandato claro: prioridade absoluta no treino de força, com cargas progressivas e exercícios multiarticulares. O ACSM recomenda 2-3 sessões semanais, cobrindo todos os grandes grupos musculares, com cargas que permitam 8-12 repetições, e progressão consistente. Nada diferente do que já fazemos — mas com uma urgência maior quando o aluno está em uso de GLP-1.
A mensagem prática
A ciência mais recente sobre canetas emagrecedoras e massa muscular conta uma história em três atos.
Primeiro ato: os números que circulam estão inflados. Massa livre de gordura não é sinônimo de músculo esquelético. Parte da perda reportada é obrigatória e vem do próprio tecido adiposo. A perda real de proteína muscular é uma fração do que as manchetes sugerem. E a proporção de perda com GLP-1 é similar à de qualquer outro método de emagrecimento.
Segundo ato: a preocupação não é infundada, mas tem nuances. A perda absoluta de músculo existe e pode ser clinicamente relevante, especialmente em populações vulneráveis. E há evidências de que o músculo que fica pode ser qualitativamente melhor — mais eficiente, menos infiltrado de gordura, mais funcional.
Terceiro ato — e este é o mais importante: para as populações que mais estão usando esses medicamentos fora da indicação original — mulheres com leve sobrepeso, mulheres na perimenopausa e menopausa, pessoas com IMC normal — simplesmente não temos dados. A ciência estudou obesos. O uso está acontecendo em todo mundo.
Para o personal trainer, a conclusão é dupla. Por um lado, você pode tranquilizar o aluno que tem indicação clínica real e está preocupado com a "destruição" muscular: a proporção de perda é normal, e com treino de força e proteína adequada, é possível preservar e até melhorar a função muscular durante o tratamento. Por outro, você precisa ser honesto com quem não tem indicação: não sabemos o que acontece com você. E na ausência de dados, a prudência manda ser conservador.
Em ambos os cenários, treino de força não é opcional. É a variável mais importante que você controla.
Se você quer se aprofundar na prescrição de treinos baseada em evidência para diferentes populações — incluindo mulheres na menopausa, pessoas em processo de emagrecimento, e pacientes em uso de medicamentos — conheça o Método Lund. É a formação mais completa para personal trainers que querem se diferenciar pelo conhecimento e entregar resultados reais para seus alunos.
Referências
Tinsley GM, Heymsfield SB. Fundamental Body Composition Principles Provide Context for Fat-Free and Skeletal Muscle Loss With GLP-1 RA Treatments. J Endocr Soc. 2024;8(11):bvae164. https://doi.org/10.1210/jendso/bvae164
Mechanick JI, Butsch WS, Christensen SM, et al. Strategies for minimizing muscle loss during use of incretin-mimetic drugs for treatment of obesity. Obes Rev. 2024;26(1):e13841. https://doi.org/10.1111/obr.13841
De Girolamo G, Sangineto M, Di Gioia G, et al. Muscle health in the modern era of incretin-based therapies. Eur J Clin Invest. 2025;56(1):e70155. https://doi.org/10.1111/eci.70155
Alissou M, Demangeat T, Folope V, et al. Impact of Semaglutide on fat mass, lean mass and muscle function in patients with obesity (SEMALEAN). Diabetes Obes Metab. 2025;28(1):112-121. https://doi.org/10.1111/dom.70141
Bhandarkar A, Bhat S, Kapoor N. Effect of GLP-1 receptor agonists on body composition. Curr Opin Endocrinol Diabetes Obes. 2025;32(6):279-285. https://doi.org/10.1097/MED.0000000000000934
Bosy-Westphal A, Kahlhöfer J, Lagerpusch M, Skurk T, Müller MJ. Deep body composition phenotyping during weight cycling: relevance to metabolic efficiency and metabolic risk. Obes Rev. 2015;16 Suppl 1:36-44. https://doi.org/10.1111/obr.12254
Hierholzer J, Benson H, Ewida HA, Ahmed MS. Mitigating loss of lean muscle in GLP-1 and dual GLP-1/GIP agonists: Pipeline opportunities and limitations. Biochim Biophys Acta Mol Basis Dis. 2026;1872(4):168172. https://doi.org/10.1016/j.bbadis.2026.168172
von Haehling S, Sato R, Langer H, et al. Muscle Loss in Obesity Therapy as a Therapeutic Target: Trial Design and Endpoints for Regulatory Discussions. J Cachexia Sarcopenia Muscle. 2025;16(6):e70147. https://doi.org/10.1002/jcsm.70147
Nikolaeva A, Vandeputte M. Subocclusive ileus following off-label high-dose semaglutide use. Endocrinol Diabetes Metab Case Rep. 2025;2025(4). https://doi.org/10.1530/EDM-25-0081
Tufail E, Sanyal S, Mithal A, Sanyal S, Chattopadhyay N. The role of glucagon-like peptides in osteosarcopenia. J Endocrinol. 2025;264(2). https://doi.org/10.1530/JOE-24-0210
Cortes TM, Vasquez L, Serra MC, et al. Effect of Semaglutide on Physical Function, Body Composition, and Biomarkers of Aging in Older Adults With Overweight and Insulin Resistance (protocolo). JMIR Res Protoc. 2024;13:e62667. https://doi.org/10.2196/62667
Abe T, Dankel SJ, Loenneke JP. Body Fat Loss Automatically Reduces Lean Mass by Changing the Fat-Free Component of Adipose Tissue. Obesity. 2019;27(3):357-358. https://doi.org/10.1002/oby.22393
Wang ZM, Pierson RN, Heymsfield SB. The five-level model: a new approach to organizing body-composition research. Am J Clin Nutr. 1992;56(1):19-28. https://doi.org/10.1093/ajcn/56.1.19
Lundgren JR, Janus C, Jensen SBK, et al. Healthy Weight Loss Maintenance with Exercise, Liraglutide, or Both Combined. N Engl J Med. 2021;384(18):1719-1730. https://doi.org/10.1056/NEJMoa2028198
Chaston TB, Dixon JB, O'Brien PE. Changes in fat-free mass during significant weight loss: a systematic review. Int J Obes. 2007;31(5):743-750. https://doi.org/10.1038/sj.ijo.0803483
