Introdução
Quando pensamos em treino de força, a primeira associação costuma ser estética: músculos maiores, corpo mais definido, aparência mais atlética. Alguns vão um pouco além e pensam em força funcional, saúde óssea ou prevenção de quedas. Mas poucos — incluindo muitos profissionais de Educação Física — fazem a conexão entre o músculo esquelético e a saúde do cérebro.
Essa conexão existe, é robusta, e pode mudar completamente a forma como você comunica a importância do treino de força para seus alunos.
Nas últimas décadas, um corpo crescente de evidências tem revelado que o músculo não é apenas um motor mecânico que move nossos ossos. É um órgão endócrino sofisticado que "conversa" com outros sistemas do corpo — incluindo o cérebro. E quando essa conversa é interrompida pela perda muscular ou pela inatividade física, as consequências vão muito além da fraqueza ou da dificuldade de subir escadas.
Neste artigo, vamos explorar o que a ciência mais recente diz sobre a relação entre sarcopenia e declínio cognitivo, entender os mecanismos biológicos que explicam essa conexão, e — mais importante — como essa informação pode transformar a forma como você prescreve e comunica o treino de força.
O Que os Números Dizem: Sarcopenia e Risco de Demência
Em 2024, Amini e colaboradores publicaram uma meta-análise abrangente no Ageing Research Reviews que reuniu dados de 24 estudos longitudinais. O objetivo era quantificar a associação entre sarcopenia e risco de declínio cognitivo e demência.
Os resultados foram impressionantes. Pessoas com sarcopenia apresentaram um risco 2,86 vezes maior de desenvolver doença de Alzheimer quando comparadas a pessoas sem sarcopenia. Para declínio cognitivo de forma geral, o risco foi 1,93 vezes maior. E para demência por todas as causas, o risco aumentou 1,50 vezes.
Esses números merecem atenção. Estamos falando de quase o triplo do risco de Alzheimer associado à perda de massa e função muscular. Para colocar em perspectiva: esse aumento de risco é comparável ou superior ao de muitos fatores genéticos e ambientais tradicionalmente associados à demência.
A meta-análise também revelou uma relação dose-resposta, o que fortalece a hipótese de causalidade. Quanto maior a gravidade da sarcopenia — classificada como provável ou confirmada pelos critérios do EWGSOP (European Working Group on Sarcopenia in Older People) — maior o risco de declínio cognitivo.
Mas aqui está um ponto crucial que muitos estudos anteriores negligenciavam: a função muscular parece ser mais preditiva do que a massa muscular isoladamente. Isso significa que não basta ter músculo — é preciso ter músculo que funciona bem. Um dado que reforça ainda mais a importância do treino de força, e não apenas da preservação passiva de massa magra.
Os Mecanismos Por Trás da Conexão
Se a sarcopenia aumenta o risco de declínio cognitivo, a pergunta natural é: por quê? Quais são os mecanismos biológicos que conectam o músculo ao cérebro?
Uma revisão narrativa publicada em 2022 por Oudbier e colaboradores no Journal of Gerontology: Medical Sciences sintetizou as evidências disponíveis e propôs quatro mecanismos patofisiológicos principais que explicam essa associação.
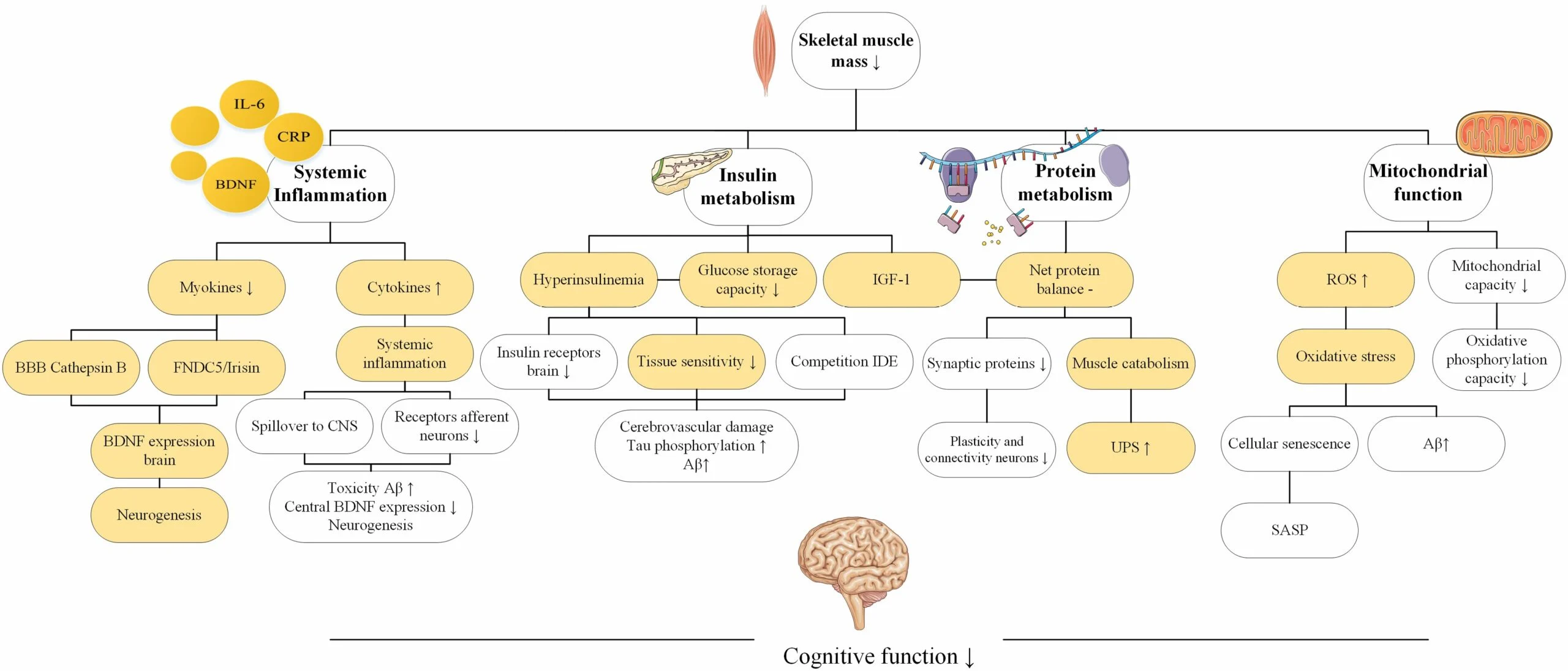
Inflamação Sistêmica
O primeiro mecanismo é a inflamação crônica de baixo grau. Com o envelhecimento e a perda muscular, há um aumento de citocinas pró-inflamatórias circulantes — moléculas como IL-6, TNF-α e proteína C-reativa que sinalizam inflamação no corpo. Essa inflamação sistêmica não fica restrita à periferia: ela atravessa a barreira hematoencefálica e contribui para neuroinflamação, um dos processos centrais na patogênese do Alzheimer.
O músculo saudável e ativo, por sua vez, tem um papel anti-inflamatório. A contração muscular durante o exercício libera miocinas com propriedades anti-inflamatórias, ajudando a contrabalançar o estado inflamatório crônico. Quando perdemos músculo ou nos tornamos sedentários, perdemos também esse efeito protetor.
Resistência à Insulina
O segundo mecanismo envolve o metabolismo da glicose. O músculo esquelético é o principal destino da glicose após as refeições — estima-se que até 80% da glicose captada do sangue em resposta à insulina seja armazenada no músculo como glicogênio. Quando há menos músculo funcional, a capacidade de "limpar" a glicose do sangue diminui, contribuindo para resistência à insulina.
E aqui está a conexão com o cérebro: o Alzheimer tem sido cada vez mais descrito como "diabetes tipo 3" por alguns pesquisadores, devido às profundas alterações no metabolismo da glicose cerebral observadas na doença. A resistência à insulina compromete o transporte de insulina através da barreira hematoencefálica e prejudica a sinalização insulínica nos neurônios — processos fundamentais para a memória e a cognição.
Acúmulo Anormal de Proteínas
O terceiro mecanismo diz respeito ao acúmulo de proteínas mal dobradas, uma característica central das doenças neurodegenerativas. No Alzheimer, as principais proteínas envolvidas são a beta-amiloide (que forma placas entre os neurônios) e a tau (que forma emaranhados dentro dos neurônios).
Pesquisas recentes sugerem que alterações na homeostase proteica muscular — incluindo disfunção nos sistemas de degradação de proteínas — podem estar relacionadas a alterações similares no cérebro. Além disso, o exercício físico demonstrou capacidade de aumentar a depuração de beta-amiloide do cérebro, possivelmente através da melhora do sistema glinfático (o sistema de "limpeza" cerebral que funciona principalmente durante o sono).
Disfunção Mitocondrial
O quarto mecanismo envolve as mitocôndrias, as "usinas de energia" das células. Tanto o músculo quanto o cérebro são tecidos altamente dependentes de energia, e ambos são particularmente vulneráveis à disfunção mitocondrial.
Com o envelhecimento e a inatividade, a função mitocondrial declina em ambos os tecidos. Mitocôndrias disfuncionais produzem menos ATP (energia) e mais espécies reativas de oxigênio (radicais livres), criando um ambiente de estresse oxidativo que danifica proteínas, lipídios e DNA. Esse processo contribui tanto para a atrofia muscular quanto para a neurodegeneração.
O exercício, por outro lado, é um dos estímulos mais potentes que conhecemos para a biogênese mitocondrial — o processo de criação de novas mitocôndrias saudáveis. E esse efeito não se limita ao músculo: existem evidências de que miocinas liberadas durante o exercício podem estimular a função mitocondrial em outros tecidos, incluindo o cérebro.
O Músculo Como Órgão Endócrino: As Miocinas
Para entender completamente a conexão músculo-cérebro, precisamos abandonar a visão do músculo como um tecido puramente mecânico. O músculo esquelético é, na verdade, o maior órgão endócrino do corpo humano.
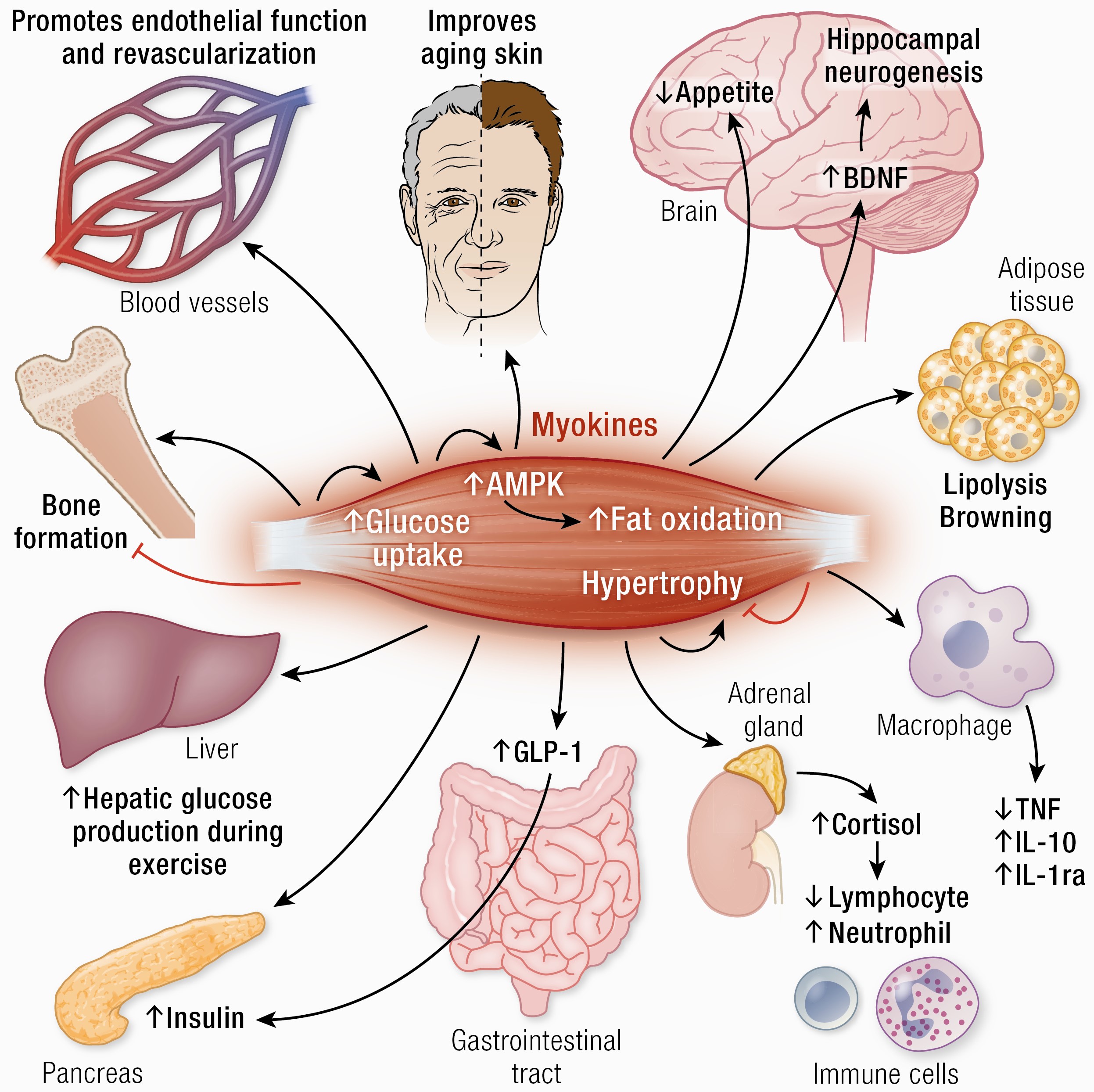
Cada vez que você contrai seus músculos — seja numa sessão de treino de força ou num exercício aeróbio — eles liberam centenas de moléculas bioativas chamadas miocinas. Essas miocinas não ficam restritas ao músculo: elas entram na circulação sanguínea e "conversam" com outros órgãos, incluindo o fígado, o tecido adiposo, os ossos, o sistema cardiovascular e — crucialmente — o cérebro.
BDNF: O Fertilizante do Cérebro
Entre as miocinas mais estudadas está o BDNF (fator neurotrófico derivado do cérebro). Apesar do nome, o BDNF é produzido tanto no cérebro quanto no músculo, e os níveis circulantes aumentam significativamente após o exercício.
O BDNF atua como um "fertilizante" para os neurônios: ele promove a sobrevivência de neurônios existentes, estimula o crescimento de novos neurônios e sinapses (neurogênese e sinaptogênese), e fortalece as conexões neurais importantes para a memória e o aprendizado. Níveis baixos de BDNF estão associados a depressão, declínio cognitivo e maior risco de demência.
Catepsina B: Atravessando a Barreira
Outra miocina de particular interesse é a catepsina B. Estudos em modelos animais demonstraram que a catepsina B produzida pelo músculo durante o exercício consegue atravessar a barreira hematoencefálica e atuar diretamente no hipocampo — a região cerebral central para a formação de memórias.
Em humanos, níveis elevados de catepsina B após programas de exercício foram associados a melhor desempenho em testes de memória.
Irisina: A Mensageira do Exercício
A irisina é outra miocina que tem recebido atenção crescente. Ela é liberada durante a contração muscular e parece ter efeitos neuroprotetores, incluindo a capacidade de estimular a expressão de BDNF no cérebro.
Estudos recentes sugerem que a irisina pode ter papel na proteção contra a patologia do Alzheimer, embora os mecanismos exatos ainda estejam sendo investigados.
A Espiral Negativa da Inatividade
Aqui chegamos a um conceito fundamental para a comunicação com seus alunos: a inatividade física não é simplesmente a ausência de benefícios do exercício. A inatividade é, em si mesma, um estado patológico que desencadeia uma cascata de deterioração.
Como Peter Attia colocou de forma eloquente ao discutir essa literatura: "O exercício é a ferramenta mais eficaz que temos para retardar a deterioração da saúde e estender a expectativa de vida." A inatividade, por outro lado, não é neutra — ela prejudica ativamente os processos fisiológicos que mantêm nossa saúde.
Quando uma pessoa se torna sedentária, a secreção de miocinas diminui. Essa diminuição interrompe a comunicação entre órgãos — o "crosstalk" que mantém os sistemas funcionando de forma integrada. O resultado é o que os pesquisadores chamam de "espiral negativa": menos movimento leva a menos miocinas, que leva a mais inflamação, pior metabolismo da glicose, declínio mitocondrial — e todos esses processos retroalimentam a perda muscular e o declínio cognitivo.
É um ciclo vicioso onde cada componente piora os demais. E o mais preocupante: esse ciclo pode começar muito antes de a pessoa perceber qualquer sintoma cognitivo ou fraqueza significativa.
A Questão da Causalidade
Uma pergunta legítima que seus alunos mais céticos podem fazer é: "Mas será que é a sarcopenia que causa o declínio cognitivo, ou pessoas com declínio cognitivo simplesmente se movem menos e por isso perdem músculo?"
É uma pergunta excelente, e a resposta honesta é que a relação é provavelmente bidirecional. Sabemos que a demência pode afetar os neurônios motores e levar a perda muscular. Ao mesmo tempo, as evidências mecanísticas que discutimos — inflamação, resistência à insulina, disfunção mitocondrial, redução de miocinas — fornecem caminhos plausíveis pelos quais a perda muscular pode contribuir para o declínio cognitivo.
O que sabemos com certeza é que:
A associação é forte, consistente e dose-dependente (quanto maior a sarcopenia, maior o risco cognitivo), como demonstram múltiplas meta-análises. Existem mecanismos biológicos plausíveis ligando músculo e cérebro. Estudos de intervenção mostram que o exercício — especialmente o treino de força — melhora tanto a função muscular quanto a função cognitiva em idosos.
A Lancet Commission on Dementia Prevention estimou que até 40% dos casos de demência podem ser atribuídos a fatores de risco modificáveis. A inatividade física está entre esses fatores. E o treino de força, ao preservar e melhorar a função muscular, pode ser uma das intervenções mais poderosas que temos disponíveis.
O Que Isso Significa Para a Prescrição
Para o profissional de Educação Física, essas evidências reforçam algo que muitos já intuíam: o treino de força não é um acessório opcional para quem "quer ficar forte" ou "definido". É uma intervenção de saúde com impacto potencial sobre o sistema mais complexo e precioso do corpo humano — o cérebro.
A prescrição de exercícios com foco na saúde cognitiva deve incluir treino de força progressivo como pilar central. Exercícios multiarticulares que desafiem grandes grupos musculares são particularmente importantes, não apenas pelo estímulo mecânico, mas pela maior liberação de miocinas associada ao recrutamento de grandes massas musculares.
A progressão de carga ao longo do tempo é fundamental. Lembre-se: a função muscular parece ser mais preditiva de risco cognitivo do que a massa isoladamente. Músculos fortes — não apenas grandes — são o objetivo.
A frequência mínima de 2 sessões semanais é recomendada, mas frequências maiores podem trazer benefícios adicionais para a secreção crônica de miocinas e os efeitos metabólicos do exercício.
A combinação com atividades aeróbias otimiza os benefícios. O exercício aeróbio tem seus próprios efeitos neuroprotetores, incluindo melhora do fluxo sanguíneo cerebral e efeitos positivos sobre o sistema glinfático.
E talvez o mais importante: começar cedo e manter a consistência. A prevenção é muito mais eficaz que a tentativa de reverter perdas estabelecidas. Cada década de treino consistente é um investimento na saúde cognitiva futura.
Como Comunicar Isso Para Seus Alunos
Esse conhecimento transforma a narrativa do treino de força. Para muitos alunos — especialmente mulheres acima de 40 anos, que são frequentemente sub-representadas nas academias de musculação — a estética pode não ser motivação suficiente. Mas a saúde cognitiva? A possibilidade de reduzir significativamente o risco de Alzheimer? Isso muda a conversa completamente.
Você pode dizer: "Quando você faz esse levantamento terra, não está apenas fortalecendo suas costas e pernas. Você está liberando moléculas que atravessam a barreira do seu cérebro e ajudam a proteger sua memória."
Ou: "Esse treino de força não é só para você ter mais energia hoje. É um investimento na sua independência cognitiva daqui a 20, 30 anos."
Para alunos com histórico familiar de demência, essa informação pode ser particularmente poderosa e motivadora. O sentimento de impotência diante de uma história genética preocupante pode ser transformado em agência: "Há algo concreto que posso fazer para modificar meu risco."
O Papel do Treino AI
Quando a base científica da prescrição já está resolvida, você tem mais tempo e energia para entregar o que realmente faz a diferença: a conexão humana, a educação sobre o porquê do treino, a motivação que transforma exercício em hábito de vida.
O Treino AI automatiza a estruturação do programa — exercícios multiarticulares fundamentais, progressão de carga baseada em evidências, volume adequado para cada nível — permitindo que você foque no acompanhamento individualizado. O sistema monitora as respostas de PSE/RIR que o aluno registra no app, ajustando a progressão de forma inteligente e evitando tanto a estagnação quanto o overtraining.
Para alunas na faixa dos 40-60 anos — população que mais se beneficia dessas informações sobre saúde cognitiva — o Treino AI considera as particularidades fisiológicas dessa fase, incluindo as mudanças hormonais da perimenopausa e menopausa que afetam tanto o músculo quanto o cérebro.
Conclusão
A conexão entre músculo e cérebro não é mais especulação — é ciência consolidada com mecanismos bem caracterizados. A sarcopenia quase triplica o risco de Alzheimer, e os caminhos biológicos que explicam essa associação revelam o músculo como um órgão endócrino central para a saúde sistêmica.
Para o profissional de Educação Física, esse conhecimento é ao mesmo tempo uma responsabilidade e uma oportunidade. Responsabilidade porque agora sabemos que o treino de força tem implicações que vão muito além da estética. Oportunidade porque essa informação pode transformar a adesão de alunos que antes não viam sentido em "pegar peso".
O músculo não é apenas o motor que move seus ossos. É um órgão que conversa com seu cérebro, que regula seu metabolismo, que modula sua inflamação. Cuidar do músculo é cuidar do corpo inteiro — incluindo o órgão que define quem você é.
E isso começa com uma série de agachamento.
Referências
Amini N, Pinter JM, Guthrie GH, et al. Association between sarcopenia and cognitive impairment and dementia: A systematic review and meta-analysis of longitudinal observational studies. Ageing Res Rev. 2024;98:102315. https://pubmed.ncbi.nlm.nih.gov/38715252/
Oudbier SJ, Goh J, Looijaard SMLM, Reijnierse EM, Meskers CGM, Maier AB. Pathophysiological Mechanisms Explaining the Association Between Low Skeletal Muscle Mass and Cognitive Function. J Gerontol A Biol Sci Med Sci. 2022;77(10):1959-1968. https://pubmed.ncbi.nlm.nih.gov/35661882/
Arosio B, Calvani R, Ferri E, et al. Sarcopenia and Cognitive Decline in Older Adults: Targeting the Muscle-Brain Axis. Nutrients. 2023;15(8):1853. https://pubmed.ncbi.nlm.nih.gov/37111070/
Jo D, Yoon G, Song J. A new paradigm in sarcopenia: Cognitive impairment caused by imbalanced myokine secretion and vascular dysfunction. Biomed Pharmacother. 2022;147:112636. https://pubmed.ncbi.nlm.nih.gov/35051857/
Livingston G, Huntley J, Sommerlad A, et al. Dementia prevention, intervention, and care: 2020 report of the Lancet Commission. Lancet. 2020;396(10248):413-446.
Giudice J, Taylor JM. Muscle as a paracrine and endocrine organ. Curr Opin Pharmacol. 2017;34:49-55.
Fiuza-Luces C, Garatachea N, Berger NA, Lucia A. Exercise is the Real Polypill. Physiology (Bethesda). 2013;28(5):330-358.
Se você quer aprender a usar ciência na prática para prescrever treinos mais assertivos para seus alunos, conheça o Método Lund.
