Nos artigos anteriores desta série, discutimos a farmacologia dessas medicações, o problema do reganho de peso e a questão da perda de massa muscular. Mas existe uma pergunta que quase ninguém faz, e que talvez seja a mais importante de todas: o que acontece quando a pessoa para?
Não estou falando do reganho em si, que já cobrimos. Estou falando de algo mais básico: existe algum protocolo para parar? Alguma orientação sobre como reduzir a dose? Algum estudo que tenha testado a melhor estratégia de saída?
A resposta, até fevereiro de 2026, é surpreendentemente curta: não.
O problema que ninguém quer discutir
Até esta data, nenhum ensaio clínico randomizado testou formalmente a redução gradual de dose versus a interrupção abrupta de semaglutida, tirzepatida ou liraglutida para tratamento de obesidade. Nenhum. Isso significa que toda pessoa que para de usar a caneta está, do ponto de vista científico, fazendo um experimento sem protocolo.
A FDA, a EMA e a OMS reconhecem essa lacuna. As bulas aprovadas pela FDA para Wegovy, Zepbound e Saxenda não contêm nenhuma instrução sobre desmame ou duração máxima do tratamento. A única regra de parada que existe é a do Saxenda: descontinuar se a perda for inferior a 4% em 16 semanas, mas essa é uma regra de eficácia, não de saída.
A OMS, em sua primeira diretriz sobre agonistas de GLP-1 para obesidade publicada em dezembro de 2025, recomendou uso contínuo por pelo menos 6 meses, reconheceu a descontinuação como lacuna crítica de conhecimento e declarou a evidência "insuficiente" para uma recomendação formal sobre como parar. A EMA segue posição semelhante: nenhuma orientação sobre redução gradual.
Ou seja, temos medicações que produzem perdas de 15% a 25% do peso corporal, que estão sendo prescritas para milhões de pessoas, e não existe um manual de saída.
Os números do reganho: o que os grandes estudos mostram
Se não existe protocolo de saída, o que sabemos é o que acontece quando a pessoa simplesmente para. E os dados são consistentes em uma direção: o peso volta.
No STEP 1 Extension, 1.961 adultos perderam em média 17,3% do peso com semaglutida 2,4 mg ao longo de 68 semanas. Após a interrupção, os participantes recuperaram aproximadamente dois terços do peso perdido em 52 semanas. E não foi só o peso: todos os marcadores cardiometabólicos que haviam melhorado — pressão arterial, glicemia, perfil lipídico — reverteram em direção ao baseline (Wilding et al., 2022).
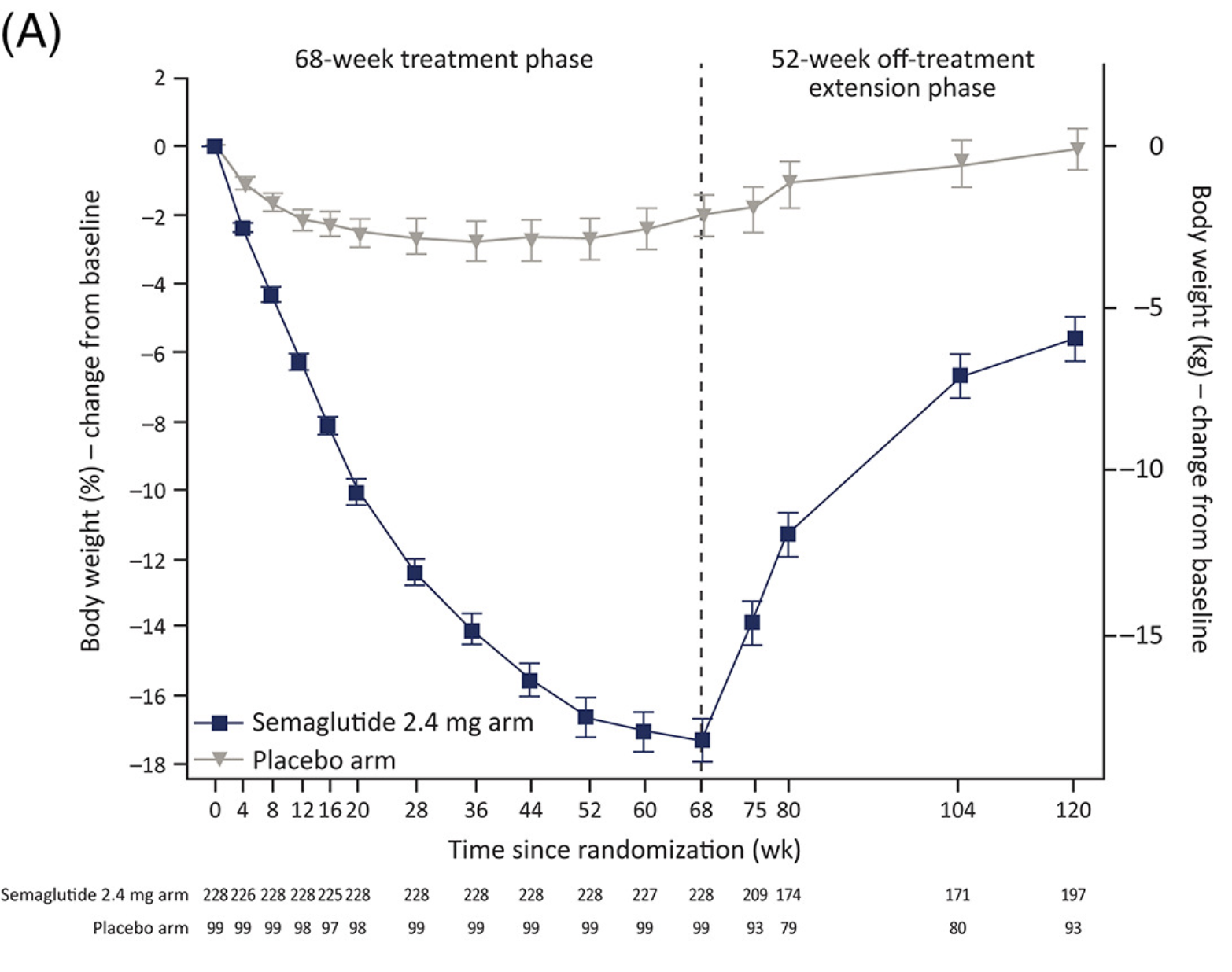
Mudança percentual no peso corporal ao longo de 120 semanas no STEP 1 Extension. A linha tracejada na semana 68 marca a interrupção da semaglutida. Adaptado de Wilding et al. (2022).
O STEP 4 testou um desenho diferente: após 20 semanas de tratamento com semaglutida (perda média de 10,6%), metade dos participantes continuou o medicamento e metade trocou para placebo. O grupo que parou recuperou 6,9% do peso em 48 semanas, ou seja, cerca de metade de tudo que havia perdido. Enquanto isso, quem continuou perdeu mais 7,9% (Rubino et al., 2021).
Com tirzepatida, o cenário é semelhante. O SURMOUNT-4 mostrou que após uma perda de 20,9%, quem interrompeu o tratamento recuperou 14,0% em 52 semanas. A perda líquida caiu para apenas 9,9%, contra 25,3% de quem continuou (Aronne et al., 2024). Uma análise post-hoc desses mesmos dados revelou que 82,5% dos pacientes que pararam a tirzepatida recuperaram pelo menos um quarto do peso perdido em um ano. Quem recuperou mais de 75% apresentou aumento de 14,7 cm na cintura e 10,4 mmHg na pressão sistólica (Horn et al., 2026).
Os números variam entre os estudos, mas o padrão é o mesmo: independente da medicação, parar significa recuperar.
A meta-análise que consolidou a evidência
Em janeiro de 2026, West et al. publicaram no BMJ a maior revisão sistemática já feita sobre o tema: 37 estudos, 9.341 participantes, cobrindo desde medicações mais antigas como orlistate até os GLP-1 RAs mais recentes.
Os achados principais foram diretos. Para semaglutida e tirzepatida especificamente, o reganho médio foi de 0,8 kg por mês após a interrupção. Nesse ritmo, a projeção é de retorno ao peso basal em aproximadamente 18 meses. Mas talvez o dado mais impactante seja a comparação: o reganho pós-medicamento é quase 4 vezes mais rápido do que o reganho após programas comportamentais de perda de peso (dieta e exercício).
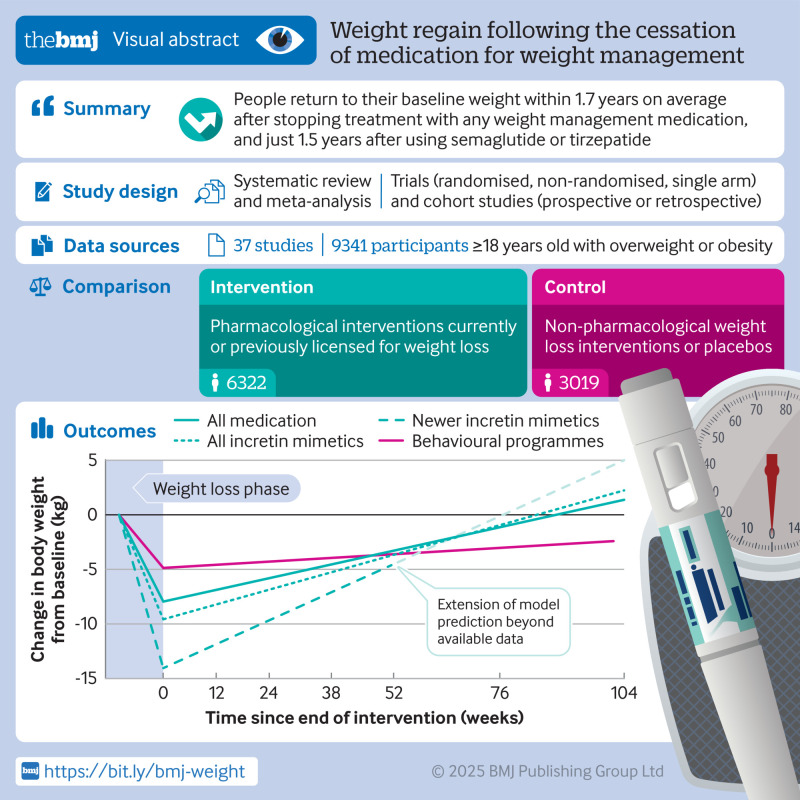
Trajetória de peso após interrupção de semaglutida e tirzepatida: reganho de 0,8 kg/mês com projeção de retorno ao peso inicial em ~18 meses. Adaptado de West et al., BMJ (2026).
Pense nisso por um momento. Uma pessoa que emagrece com dieta e exercício, se parar tudo, recupera o peso de forma gradual ao longo de anos. Uma pessoa que emagrece com medicação e para, recupera na velocidade de meses. A meta-análise também mostrou que não é só o peso: marcadores como hemoglobina glicada, pressão sistólica e colesterol retornam ao baseline em cerca de 1,4 anos.
Os autores de Oxford foram claros na conclusão: apesar do sucesso em produzir perda de peso inicial, essas medicações isoladamente podem não ser suficientes para controle de peso a longo prazo.
Por que o corpo recupera tudo?
Para entender o reganho, é preciso entender o que a medicação faz e o que ela não faz.
Os agonistas de GLP-1 atuam principalmente no sistema nervoso central, reduzindo a fome e aumentando a saciedade. Em 2024, Kim et al. publicaram na Science um estudo que mapeou os neurônios específicos no tronco cerebral que medeiam o efeito de saciedade da semaglutida. Quando a medicação é retirada, esses circuitos voltam ao estado anterior. A fome retorna. A saciedade diminui. E o corpo, que biologicamente interpreta a perda de peso como uma ameaça, ativa todos os mecanismos de defesa que pode.
Esses mecanismos incluem a redução da taxa metabólica basal proporcional à perda de massa, a supressão de hormônios de saciedade como leptina e PYY, o aumento de grelina (o hormônio da fome), adaptações hipotalâmicas que recalibram o "set point" de peso, e a perda do efeito direto da medicação sobre o esvaziamento gástrico. É uma tempestade perfeita de biologia trabalhando contra a manutenção.
Um dado particularmente preocupante vem de Jeromson et al. (2025): após descontinuação de semaglutida em modelo pré-clínico, o reganho de peso foi predominantemente em forma de gordura, com recomposição desproporcional de tecido adiposo. Isso se conecta diretamente com o que discutimos no artigo sobre massa muscular: a pessoa perde peso que inclui músculo e gordura, mas recupera predominantemente gordura. Cada ciclo piora a composição corporal.
E se a resposta for simplesmente não parar?
Existe um elefante na sala que precisa ser nomeado: talvez a pergunta certa não seja "como parar?" mas sim "por que parar?"
Ninguém pergunta a um hipertenso quando ele vai parar de tomar o anti-hipertensivo. Ninguém questiona por quanto tempo um diabético tipo 2 vai usar metformina. Ninguém espera que uma pessoa com colesterol alto faça um "desmame" de estatina depois de atingir os valores-alvo. A expectativa, tanto médica quanto social, é de que essas medicações sejam contínuas, porque tratam doenças crônicas.
A obesidade, pela definição de todas as grandes sociedades médicas do mundo, é uma doença crônica. A fisiopatologia é clara: existem mecanismos biológicos ativos que defendem o excesso de gordura corporal, da mesma forma que existem mecanismos que mantêm a pressão arterial elevada ou a glicemia desregulada. A medicação corrige uma disfunção enquanto está sendo usada. Quando é retirada, a disfunção retorna. Isso não é falha do paciente. É biologia.
O problema é que a obesidade ainda não recebe o mesmo tratamento cultural que outras doenças crônicas. Existe uma expectativa implícita de que a pessoa deveria "aprender a se controlar" e não precisar mais do medicamento, uma expectativa que não fazemos com nenhuma outra condição crônica. Se um paciente usa losartana há 10 anos e a pressão está controlada, ninguém diz "já está na hora de parar e manter a pressão baixa sozinho." Todo mundo entende que a pressão está controlada porque ele toma a medicação.
A AACE, em seu consenso de 2025, foi explícita: a gordura corporal é biologicamente defendida e a descontinuação de medicações que atuam nesses mecanismos resulta em reganho esperado (Nadolsky et al., 2025). O ACC reforçou que o tratamento deve ser de longo prazo (ACC Expert Consensus, 2025). A ADA, nos Standards of Care 2025-2026, declarou que a descontinuação súbita frequentemente resulta em reganho e piora dos fatores de risco cardiometabólico (Recomendação 8.19, Grau A). Pela primeira vez, a edição 2026 mencionou a possibilidade de manutenção com a menor dose efetiva ou terapia intermitente.
A exceção parcial é o NICE britânico, que recomenda uso máximo de 2 anos para semaglutida, uma posição cada vez mais isolada entre os órgãos regulatórios globais.
A mensagem da ciência é convergente: para muitos pacientes, a resposta mais honesta pode ser que a medicação faz parte do tratamento de longo prazo, assim como em qualquer outra doença crônica. Isso não significa que todos precisarão usar para sempre. Significa que a decisão de parar deveria ser individualizada, baseada em evidência, e acompanhada de perto, não motivada por pressão social ou pela ideia de que precisar de medicação é algum tipo de fracasso.
E é exatamente aqui que o papel do profissional de Educação Física se torna central. Porque mesmo para quem vai continuar usando, o exercício muda tudo: melhora a composição corporal, preserva massa muscular, permite eventualmente reduzir a dose, e constrói uma base de saúde metabólica que a medicação sozinha não consegue construir.
O único dado sobre desmame gradual
Para os pacientes que, por qualquer razão, vão de fato interromper o tratamento, existe um estudo que chegou mais perto de testar a ideia de redução gradual: o estudo Embla, liderado por Gudbergsen e apresentado no Congresso Europeu de Obesidade em 2024. Trata-se de um estudo observacional dinamarquês com 2.246 indivíduos, dos quais 353 pacientes que desejavam parar a semaglutida após atingir seu peso-alvo foram submetidos a redução gradual da dose ao longo de 9 semanas em média, combinada com coaching de exercício e dieta.
Um detalhe importante: a dose máxima média utilizada foi de apenas 0,77 mg, muito abaixo dos 2,4 mg padrão para obesidade. Dos 240 que completaram o desmame até dose zero, 85 foram acompanhados por 26 semanas. O resultado foi encorajador: o peso permaneceu estável, com perda adicional média de 1,5%. Apenas 19% precisaram reiniciar a semaglutida, com ganho médio de apenas 1,3% entre a cessação e a reintrodução.
Esses resultados são interessantes, mas precisam de contexto. É um estudo observacional, não randomizado. A dose usada era muito menor que a padrão. O acompanhamento foi curto. E os pacientes tinham suporte comportamental ativo, incluindo coaching de exercício. Ainda assim, é o dado mais próximo que temos de uma estratégia de saída, e sugere que a combinação de doses baixas, redução gradual e suporte comportamental pode funcionar para um subgrupo de pacientes.
O estudo que muda tudo para o personal trainer
Se existe um estudo que deveria ser leitura obrigatória para todo profissional de Educação Física que atende alunos usando canetas, é o S-LiTE.
Publicado no New England Journal of Medicine por Lundgren et al. (2021), o S-LiTE randomizou adultos com obesidade para quatro grupos após uma dieta de baixa caloria: exercício supervisionado + placebo, liraglutida + atividade habitual, exercício supervisionado + liraglutida, ou placebo + atividade habitual. Após 1 ano de tratamento, tudo foi interrompido. Todas as medicações, todos os programas.
O follow-up de 1 ano após a interrupção, publicado por Jensen et al. (2024), é onde a história fica realmente interessante. Quem havia feito exercício combinado com liraglutida teve 4,2 vezes mais chance de manter pelo menos 10% de perda de peso comparado com quem usou apenas liraglutida. E 7,2 vezes mais chance comparado com placebo. O grupo que fez apenas exercício também se saiu melhor que o placebo, com 3,7 vezes mais chance de manter a perda.
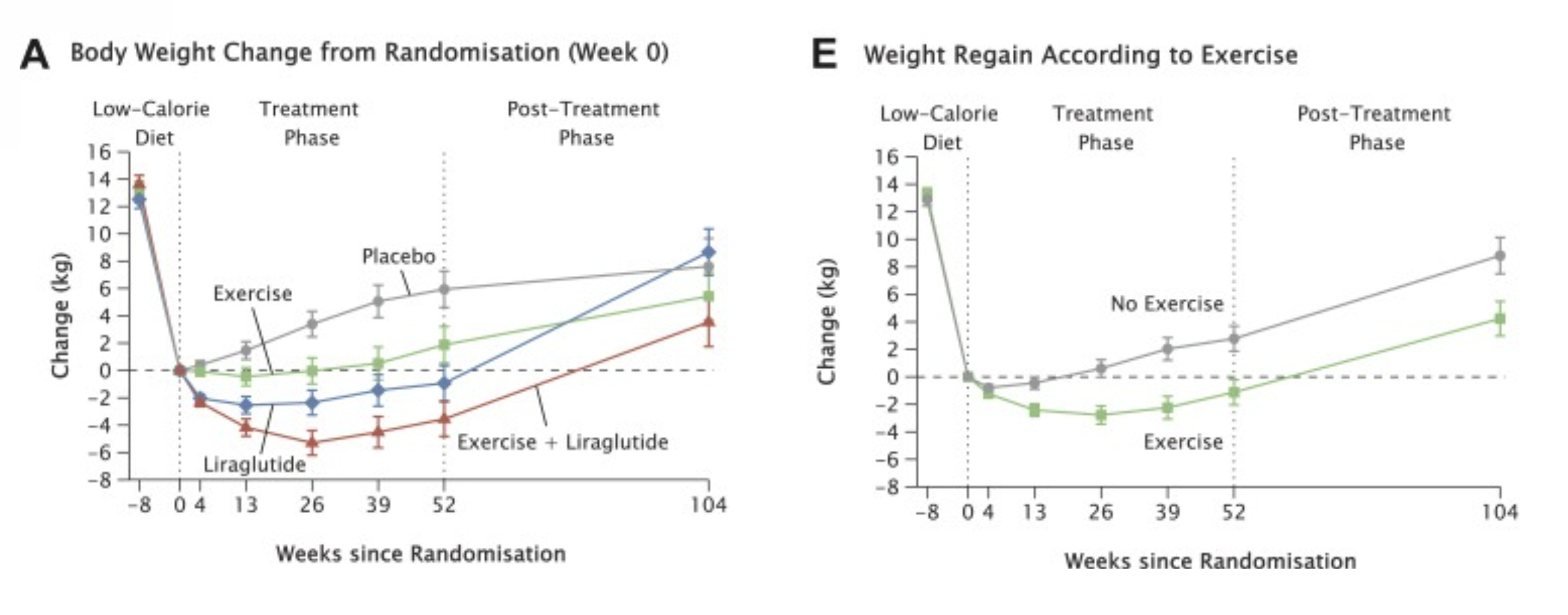
Mudança de peso corporal ao longo de 104 semanas no S-LiTE. Após a interrupção (semana 52), o grupo que combinou exercício com liraglutida manteve significativamente mais perda de peso. Adaptado de Jensen et al. (2024).
Mas o dado mais revelador talvez seja comportamental: um ano depois de tudo ter sido interrompido, o grupo que havia feito exercício supervisionado mantinha uma média de 240 minutos de atividade física por semana. O grupo que usou apenas liraglutida? 30 minutos por semana. O exercício criou um hábito. A medicação, sozinha, não.
O mecanismo é duplo. Primeiro, o exercício aumenta a produção endógena de GLP-1 pelo próprio intestino, criando uma compensação biológica parcial quando a medicação é retirada. Segundo, e talvez mais importante, ele constrói comportamentos e rotinas que persistem independentemente da farmacologia.
O que isso significa para você
Se você é personal trainer e atende alunos que usam ou já usaram canetas emagrecedoras, a mensagem desta série é clara: você não é um coadjuvante nesse processo. Você é, potencialmente, o fator decisivo entre uma perda de peso temporária e uma mudança sustentável.
O S-LiTE é evidência de nível 1 — ensaio clínico randomizado publicado no NEJM — de que treino supervisionado durante o uso de GLP-1 RA é o que determina se a perda de peso sobrevive à retirada do medicamento. E para quem vai continuar usando a medicação de forma crônica, como a ciência cada vez mais sugere ser o caminho para muitos pacientes, o exercício continua sendo indispensável: ele preserva massa muscular, melhora a composição corporal, potencializa os efeitos metabólicos e pode até permitir que o médico reduza a dose ao longo do tempo.
A janela de oportunidade está no período em que o aluno está tomando a medicação. É ali, enquanto a fome está controlada e a motivação está alta, que ele precisa construir com você a infraestrutura que vai sustentá-lo, independentemente de ele parar ou continuar o medicamento.
Isso significa prescrever treino de força para preservar massa muscular durante a perda de peso. Significa progredir carga de forma consistente para que os ganhos de força sejam reais. Significa criar uma rotina de exercícios que o aluno consiga e queira manter por conta própria. E significa ter o conhecimento para explicar ao aluno, e ao médico dele, por que o exercício não é opcional nessa equação.
Porque os dados não deixam dúvida: seja a caneta temporária ou permanente, quem constrói o resultado é o treino.
Se você quer aprender a prescrever treinos baseados em evidência para populações como essa, com a profundidade científica que esse tema exige, conheça o Método Lund — a formação mais completa para personal trainers que querem se diferenciar pelo conhecimento.
